
6 may | 6.00 pm
Bio Pharma Day is a career ecosystem organized by Jobadvisor, dedicated to job, training and orientation opportunities in the bio, pharma, medtech industries. It is designed for students, graduates and early-career professionals who want to connect with leading companies.
🧬🎓 In 2026, Bio Pharma Day includes 2 virtual fairs and 2 onsite events in Milan and Rome, dedicated to profiles with backgrounds in life sciences and healthcare, including biomedical and medical engineering.
The program also features dedicated virtual fairs specifically for: 💊 pharmacy & CTF graduates, 🩺 medical doctors interested in the pharma industry, ⚙️ and STEM profiles.
💡 Bio Pharma Day also offers expert-led meetings to support career orientation and personal development.
Are you a Company willing to attend?
For more information or a quotation, please contact us:
T: + 39 393 92.55.808
E: biopharmaday@jobadvisor.it
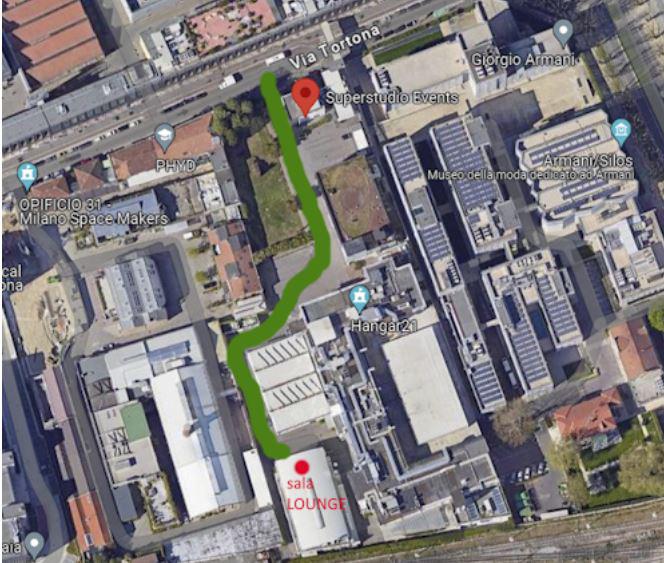
The event will be held at Superstuido Events, via Tortona 27 - 20144 MI
in the Sala Lounge - from 10 a.m. to 5 p.m.
How to arrive: see the map

These companies will attend one or more events in 2026: discover their profile!
🟠 label: Bio Pharma Day - virtual fair on March, April, September, November
🟣 label: Bio Pharma Day in Milan (May) and/or Rome (December)
🟡 label: Recruiting Farmacisti - virtual fair on February
🔵 label: Recruiting Medici - virtual fair on June
More coming soon!

Here you will find the list of opportunities at Bio Pharma Day.
For the event in MILAN, news Opportunities have been added!
TO APPLY: check the guidelines in each job description.
If you are logged in, the first ones marked with or are close to your degree or field of studies.

🌟 Sei un/una Farmacista e vuoi fare la differenza? 🌟
Medi-Market Italia è alla ricerca di un/a farmacista per le sue Parafarmacie in:
Trentino-Alto Adige, Friuli-Venezia Giulia, Liguria, Piemonte, Lombardia, Veneto, Emilia-Romagna, Toscana, Marche e Lazio
💊 Chi cerchiamo:
💙 Chi siamo:
Il gruppo multinazionale belga Medi-Market è attivo nel campo della salute e del benessere con farmacie, parafarmacie e istituti di bellezza in Belgio, Lussemburgo, Paesi Bassi, Spagna e Italia.
Dal 2019 Medi-Market ha avviato un’ambiziosa strategia di espansione in Italia, dove oggi è presente con numerose parafarmacie distribuite sul territorio nazionale.
La nostra mission: salute e benessere alla portata di tutti!
✨ Cosa ti offriamo:
Inoltre:
💡 Inclusività:
Accogliamo candidati/e delle Categorie protette e promuoviamo le pari opportunità.
Unisciti a noi e rendi la salute e il benessere accessibili a tutti!
Ti senti la persona giusta per questa posizione?
📩 Vieni a Milano l'8 maggio per conoscerci e invia il tuo CV a: e.conti@medi-market.it e r.tarallo@medi-market.it

Il Master of International Healthcare Management, Economics and Policy (MIHMEP) è un programma di un anno full-time in lingua inglese, che riconosce 70 crediti ECTS/CFU, rivolto a coloro che desiderano assumere ruoli di responsabilità a livello globale nel settore sanitario, che si tratti di industria privata, organizzazioni governative e internazionali o fornitori di servizi sanitari.
Offriamo un approccio rigoroso e specialistico, insieme a una visione globale, per ampliare gli orizzonti del management sanitario di tutti coloro che operano nel settore. Chi partecipa al programma MIHMEP ha generalmente una formazione universitaria e svariati background culturali e professionali, apprezza la diversità culturale, è in grado di affrontare i cambiamenti, ha una forte motivazione e disponibilità ad affrontare un percorso di formazione impegnativo.
Il programma MIHMEP è l'unico Master che fonde la visione privata (aziendale) e pubblica dell'assistenza sanitaria, offrendo sia una panoramica generale che specializzazioni in tre settori:
Requisiti
Scadenze
Esoneri:
Deadline invio candidatura: 28 maggio 2026
Inizio master: 21 settembre 2026
Per fissare un colloquio individuale on campus o da remoto, visitare il nostro campus contattare:
Priscilla Gatto
Guidance & Recruitment Master Division
LinkedIn: https://www.linkedin.com/in/priscilla-gatto/
Mobile/WhatsApp +39 3426216947
Telephone: +39 02 5836 3116

Il Master in Management per la Sanità (MiMS) è il Master universitario di II livello di 12 mesi, in lingua italiana, che permetterà ai giovani talenti di acquisire e sviluppare le competenze e le abilità necessarie per una carriera di successo nelle aziende sanitarie pubbliche e private, nelle imprese fornitrici di tecnologie, nei centri di ricerca e formazione, nel mondo della consulenza nel settore della sanità.
Il Master in Management per la Sanità è un percorso formativo rivolto a giovani laureati e professionisti nelle prime fasi di carriera che vogliono sviluppare competenze manageriali per operare con efficacia in contesti sanitari complessi, fortemente regolati e ad alta intensità di innovazione.Il Master MiMS non si limita a fornirti nozioni teoriche, ma ti permette di mettere continuamente in pratica le tue competenze in un contesto professionale reale. La seconda parte del MiMS è infatti interamente dedicata al In company – project : un'esperienza formativa unica che combina lezioni frontali, testimonianze di aziende e professionisti, ricerche sul campo in collaborazione con le aziende partner, site visit e study tour ed in fine un progetto sul campo.
Requisiti
Sono prese in considerazione, inoltre:
Scadenze
Esoneri SDA:
Domanda di ammissione: 25 novembre 2026
Inizio programma: 25 gennaio 2027
Per fissare un colloquio individuale on campus o da remoto, visitare il nostro campus contattare:
Priscilla Gatto
Guidance & Recruitment Master Division
LinkedIn: https://www.linkedin.com/in/priscilla-gatto/
Mobile/WhatsApp +39 3426216947
Telephone: +39 02 5836 3116

Learn more about the companies that will attend Bio Pharma Day!
Log-in, access the content and prepare yourself for the event.
or register now if you do not have an account yet
This website uses cookies to provide a better service. To have more information, please click here. Continuing the surfing of the website, your agree with the usage of the cookies. Yes, I Agree



















































































































































